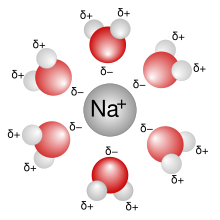
 一个被水分子溶解的钠离子
一个被水分子溶解的钠离子
溶解(英語:dissolution)又稱溶剂化(solvation)、溶劑合作用[1],是溶质分散于溶剂中而成为一个分子混合状态的溶液的过程[2]。溶剂化描述了溶剂与溶解分子的相互作用。离子化的分子和不带电的分子,都可与溶剂发生强烈的相互作用;此作用的强度和性质影响溶质的许多性质,包括溶解度、反应性和颜色,也影响溶剂的性质,如黏度和密度。
当离子溶解时,它们会散布开来并被溶剂分子包裹。离子越大,能包裹它的溶剂分子就越多。有时溶解会产生放热、吸热的现象,例如氯化铵溶于水时会吸热使液体温度降低,而氢氧化钠溶于水时会放热使溶液温度升高。一般地,稳定、单一的溶液没有廷得耳效應。
表格摘自人民教育出版社高等中学《化学》教科书
| 阳离子\阴离子 |
OH- |
NO3- |
Cl- |
SO42- |
CO32-
|
| H+ |
不存在 |
可溶、挥发 |
可溶、挥发 |
可溶 |
可溶、挥发
|
| NH4+ |
可溶、挥发 |
可溶 |
可溶 |
可溶 |
可溶
|
| K+ |
可溶 |
可溶 |
可溶 |
可溶 |
可溶
|
| Na+ |
可溶 |
可溶 |
可溶 |
可溶 |
可溶
|
| Ba2+ |
可溶 |
可溶 |
可溶 |
不溶 |
不溶
|
| Ca2+ |
微溶 |
可溶 |
可溶 |
微溶 |
不溶
|
| Mg2+ |
不溶 |
可溶 |
可溶 |
可溶 |
微溶
|
| Al3+ |
不溶 |
可溶 |
可溶 |
可溶 |
不存在
|
| Mn2+ |
不溶 |
可溶 |
可溶 |
可溶 |
不溶
|
| Zn2+ |
不溶 |
可溶 |
可溶 |
可溶 |
不溶
|
| Fe2+ |
不溶 |
可溶 |
可溶 |
可溶 |
不溶
|
| Fe3+ |
不溶 |
可溶 |
可溶 |
可溶 |
不存在
|
| Cu2+ |
不溶 |
可溶 |
可溶 |
可溶 |
不存在
|
| Ag+ |
不存在 |
可溶 |
不溶 |
微溶 |
不溶
|

